Болезнь верльгофа что это такое простыми словами
Тромбоцитопеническая пурпура
Статья проверена врачом онкогематологом, педиатром, к.м.н. Будариным М.А., носит общий информационный характер, не заменяет консультацию специалиста.
Для рекомендаций по диагностике и лечению необходима консультация врача.
В Клиническом госпитале на Яузе для диагностики тромбоцитопенической пурпуры (ТП) используются современные лабораторные и инструментальные методы обследования. В зависимости от выраженности заболевания и общего состояния пациента составляется индивидуальная схема лечения тромбоцитопенической пурпуры и дальнейшего ведения больного.
О развитии болезни
Тромбоцитопеническая пурпура (болезнь Верльгофа) — это иммунообусловленное заболевание, которое характеризуется периодическим или постоянным снижением количества тромбоцитов в периферической крови пациента (меньше 100,0×10 9 /л) и повышенным риском развития кровотечений.
Заболеваемость ТП составляет 100 тысяч детского населения и случаев на 100 тыс. взрослого населения. Чаще болеют дети в возрасте до 10 лет и молодые женщины.
Причины возникновения болезни Верльгофа не установлены, однако доказано, что снижение количества тромбоцитов связано с аутоиммунным процессом, в силу которого антитела разрушают собственные кровяные клетки. Также наблюдается снижение регенеративной активности в костном мозге. Запуск патологической реактивности ученые связывают с такими факторами, как:
В среднем от момента взаимодействия с пусковым агентом да появления первых симптомов недуга проходит около 2 недель.
Клиническая картина
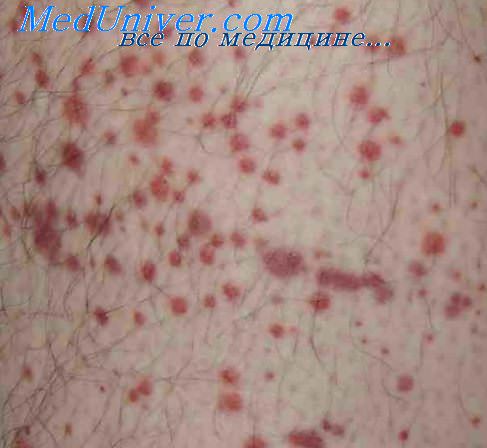
Геморрагический синдром — основное проявление заболевания. Проявляется в виде петехиальной сыпи на коже и слизистых, экхимозов («синяков»), частых и рецидивирующих носовых кровотечений, повышенной кровоточивости десен, обильной и затяжной менструации. В особо тяжелых случаях могут развиваться желудочно-кишечные кровотечения, кровоизлияния в головной мозг.
Диагностика заболевания
Консультация врача гематолога
Врач тщательно осматривает и опрашивает пациента, выясняя детально историю развития заболевания, семейный анамнез и др.
Лабораторная диагностика
Инструментальные методы
Все исследования проводятся опытными специалистами на аппаратуре экспертного класса, что обеспечивает точность диагностики.
Лечение патологии
Лечение тромбоцитопенической пурпуры направлено на:
Схема терапии разрабатывается для каждого пациента индивидуально и зависит от тяжести состояния больного, степени прогрессирования ТП.
Фармакотерапия
Применяется лечение кортикостероидами, агонистами рецепторов тромбопоэтина (стимуляция кроветворения), иммуносупрессивными препаратами, внутривенными иммуноглобулинами.
Экстракорпоральная гемокоррекция
В межприступный период в Клиническом госпитале на Яузе для лечения тромбоцитопении используются инновационные технологии экстракорпоральной гемокоррекции (ЭГ), с помощью которых из крови удаляется значительная часть аутоиммунных комплексов, что приводит к восстановлению свертывающей активности тромбоцитов и образованию функционально активных кровяных пластинок.
Могут применяться следующие методы ЭГ:
Специалисты Клинического госпиталя на Яузе отмечают: своевременное обращение к специалисту в несколько раз увеличивает вероятность быстрого достижения длительной ремиссии при тромбоцитопенической пурпуре. Не откладывайте свой визит к гематологу «на завтра» — запишитесь на прием прямо сейчас!
Цены на услуги Вы можете посмотреть в прайсе или уточнить по телефону, указанному на сайте.
Болезнь верльгофа что это такое простыми словами
Тромбоцитопеническая пурпура (болезнь Верльгофа) — наиболее часто встречающаяся форма геморрагического диатеза. Различают острую и хроническую формы болезни, которые в свою очередь подразделяются на иммунную и неиммунную. Для острой формы заболевания характерен короткий анамнез (от нескольких дней до нескольких месяцев). Болезнь Верльгофа может наблюдаться в любом возрасте, однако хронические ее формы чаще встречаются у детей. Заболевают чаще женщины.
Этиология неясная. Провоцирующими факторами являются различные инфекции, эндокринные нарушения и др.
Патогенез кровоточивости прежде всего обусловлен тромбоцитопенией. У 70% больных тромбоциты единичные или отсутствуют. Помимо количественных изменений тромбоцитов, установлены значительные качественные изменения их, особенно при хронической форме заболевания. Адгезивные свойства, присущие тромбоцитам, резко снижены. Наряду с изменениями тромбоцитов при болезни Верльгофа имеют место нарушения плазменных факторов свертывающей системы крови, обусловливающие гипокоагуляиню. Все это приводит к образованию рыхлого сгустка. Ретракция кровяного сгустка в большинстве случаев полностью отсутствует.
Отмечается повышенная проницаемость сосудистой стенки, что может проявляться резко выраженным симптомом жгута (образование петехий на коже ниже наложенного на конечность жгута) и удлинением времени кровотечения по Дуке (свыше 8 мин).
Наиболее характерным проявлением болезни Верльгофа служит геморрагический синдром — различного рода кровоизлияния н кровотечения из слизистых оболочек различных органов. Наиболее часто наблюдаются кожные кровоизлияния, сочетающиеся с кровотечением из слизистых оболочек матки, носа и десен. Опасны кровоизлияния в мозг. Обильное и продолжительное кровотечение, сопровождающееся прогрессирующей анемизацией, вызывает у ряда больных изменения сердечно-сосудистой системы и других органов. Размеры печени н селезенки, как правило, не увеличены.
Диагностика болезни Верльгофа в типичных случаях не вызывает сомнений и основывается как на характерной клинической картине, так и данных лабораторных исследований. Ошибки чаще всего обусловлены трудностями дифференциальной диагностики с другими заболеваниями, при которых также наблюдается геморрагический синдром (гипопластическая анемия, системная красная волчанка, протекающая с симптомокомплексом Верльгофа и синдромом Фишера — Эванса, болезнь Гоше).
Лечение болезни Верльгофа представляет трудную задачу и зависит от формы и стадии заболевания. Во время обострения геморрагического диатеза лечебные мероприятия должны быть направлены на остановку кровоточивости, во время ремиссии — на предупреждение рецидива болезни н сопровождающих ее осложнений. С этой целью широко применяется комплексное лечение, включающее повторные трансфузии крови, введение се препаратов и кортикостероидных гормонов. Одним нз нанболсе эффективных средств лечения болезни Верльгофа, особенно ее хронических форм, остается оперативное лечение — спленэктомия.
Механизм лечебного действия спленэктомии сложен н не до конца ясен. Причина и место разрушения тромбоцитов еще спорны, но есть указания, что в этом процессе принимают участие антитромбоцитарные антитела, образующиеся в селезенке.
Наиболее выгодным периодом для операции является фаза ремиссии. Так, по данным Л. С. Цепа, у 79% оперированных в стадии стихания геморрагических проявлений получена клинико-гематологическая и у 21%— клиническая ремиссия. Анализ непосредственных и отдаленных результатов спленэктомии позволяет считать одной из главных причин ее неудач ошибки диагностики до операции. Рецидивы у больных, подвергнутых спленэктомии, могут иметь место при преимущественном распаде тромбоцитов в печени.
Спленэктомии не даст желаемого результата и в тех случаях, когда кровоточивость связана с дисфункцией желез внутренней секреции. В рецидиве заболевания существенную роль играют инфекционные и эндокринные факторы. Смертельные исходы после спленэктомии наблюдаются у 5% больных, оперированных преимущественно в разгар геморрагии, тогда как при операциях, произведенных в фазе ремиссии, такие исходы редки.
Тромбоцитопеническая пурпура (болезнь Верльгофа). Симптомы. Диагностика. Лечение.
Этиология и патогенез
При тромбоцитопенической пурпуре тромбоцитопения развивается вследствие разрушения тромбоцитов посредством иммунных механизмов. Антитела к собственным тромбоцитам могут появляться спустя 1-3 нед после перенесённых вирусных или бактериальных инфекций, профилактических прививок, приёма лекарственных препаратов при индивидуальной их непереносимости, переохлаждения или инсоляции, после хирургических операций, травм. В ряде случаев какую-либо определённую причину выявить не удаётся. Поступившие в организм антигены (например, вирусы, лекарственные средства, в том числе вакцины) оседают на тромбоцитах больного и индуцируют иммунный ответ. Антитромбоцитарные антитела относят преимущественно к IgG. Реакция «Аг-AT» происходит на поверхности тромбоцитов. Продолжительность жизни тромбоцитов, нагруженных антителами, при тромбоцитопенической пурпуре снижена до нескольких часов вместо 7-10 дней в норме. Преждевременная гибель тромбоцитов происходит в селезёнке. Кровоточивость при тромбоцитопенической пурпуре обусловлена снижением количества тромбоцитов, вторичным повреждением сосудистой стенки в связи с выпадением ангиотрофической функции тромбоцитов, нарушением сократительной способности сосудов из-за понижения концентрации серотонина в крови, невозможностью ретракции кровяного сгустка.
Клиническая картина болезни Верльгофа
По течению выделяют острые (длительностью до 6 мес) и хронические (продолжительностью более 6 мес) формы заболевания. При первичном осмотре установить характер течения заболевания невозможно. В зависимости от степени проявления геморрагического синдрома, показателей крови в течении заболевания выделяют три периода: геморрагический криз, клиническая ремиссия и клинико-гематологическая ремиссия.
Лабораторные исследования
Характерны снижение содержания тромбоцитов в крови вплоть до единичных в препарате и увеличение времени кровотечения. Длительность кровотечения не всегда соответствует степени тромбоцитопении, так как она зависит не только от количества тромбоцитов, но и от их качественных характеристик. Значительно снижена или не наступает вообще ретракция кровяного сгустка. Вторично (в результате тромбоцитопении) изменяются плазменно-коагуляционные свойства крови, что проявляется недостаточностью образования тромбопластина в связи с дефицитом 3-го тромбоцитарного фактора. Нарушение образования тромбопластина приводит к снижению потребления протромбина в процессе свёртывания крови. В некоторых случаях при тромбоцитопенической пурпуре в период криза отмечают активацию фибринолитической системы и повышение антикоагулянтной активности (антитромбины, гепарин). У всех больных с тромбоцитопенией снижена концентрация серотонина в крови. Эндотелиальные пробы (жгута, щипка, молоточковая, уколочная) в период гематологического криза положительны. В красной крови и лейкограмме (при отсутствии кровопотерь) изменений не находят. При исследовании красного костного мозга обычно выявляют нормальное или повышенное содержание мегакариоцитов.
Диагностика и дифференциальная диагностика
Диагностика тромбоцитопенической пурпуры основана на характерной клинической картине и лабораторных данных.
Идиопатическая тромбоцитопеническая пурпура. Симптомы, диагностика и лечение ИТП
1. Что такое идиопатическая тромбоцитопеническая пурпура?
Когда немецкий врач Пауль Готлиб Верльгоф описал заболевание, которое сегодня мы называем идиопатической тромбоцитопенической пурпурой, состав крови ещё не был достаточно изучен. Лишь 150 лет спустя болезнь связали с недостатком тромбоцитов в крови.
В ряду заболеваний, характеризующихся тромбоцитопениями, термин «идиопатический» означает неизвестную причину данной патологии. Термин «пурпура» в названии болезни указывает на внешние проявления болезни: кожные точечные и пятнистые кровоизлияния, капиллярные геморрагии, экхимозы. На поверхности кожи они имеют тёмно-бордовый цвет.
Идиопатическая тромбоцитопеническая пурпура может протекать остро (до полугода) или иметь хроническое течение.
Самая высокая заболеваемость приходится на школьный и старший дошкольный возраст. Для детей в возрасте от 10 лет идиопатическая тромбоцитопеническая пурпура диагностируется в два раза чаще у девочек, чем у мальчиков.
2. Причины болезни Верльгофа
Причины возникновения ИТП однозначно не установлены. Треть больных перед началом заболевания не получает никаких воздействий, которые могли бы повлиять на здоровье. У остальных выявляется ряд факторов, которые теоретически могут считаться этиологическими, но реальная причинно-следственная связь с заболеванием для них до сих пор не доказана:
Нормальное содержание тромбоцитов в составе крови обеспечивается сбалансированностью двух постоянно протекающих процессов: образование новых тромбоцитов и разрушение их в периферическом русле. У больных идиопатической тромбоцитопенической пурпурой повышена скорость разрушения тромбоцитов.
Хотя причины такого нарушения остаются не вполне ясными, в настоящее время определённо можно сказать, что механизм, который провоцирует хроническое интенсивное разрушение тромбоцитов, носит иммунологический характер. Продолжительность жизни тромбоцитов сокращается от нескольких дней до нескольких часов. Выработка их в костном мозге остаётся на прежнем уровне. Иногда воспроизводство усиливается (как реакция на дисбаланс), однако это не компенсирует в достаточной мере тромбоцитарный дефицит. Дальнейшее течение сложных физиологических компенсаторно-иммунных процессов нередко только усиливает тромбоцитопению, поскольку к дефициту тромбоцитов добавляется их неполноценность, – что, в свою очередь, ведёт к неспособности даже существующих клеток выполнять функции свёртывания крови. Хроническая идиопатическая тромбоцитопеническая пурпура носит аутоиммунный характер. В этом случае прогнозируется пожизненное нарушение состава крови с периодами ремиссий и обострений.
Если снижение содержания тромбоцитов в крови вызвано действием какого-либо известного фактора, то при его устранении тромбоцитопения прекращается и свертываемость крови восстанавливается. Такая форма заболевания считается острой и имеет благоприятный прогноз.
Первичная манифестация заболевания в виде кожных кровоизлияний происходит при снижении содержания тромбоцитов до 30–50 х 109/л. Кровотечения из носа и слизистых начинаются при 20–30 х 109/л. Если показатели тромбоцитов снижаются до 10 х 109/л и меньше, возникает серьёзная опасность геморрагического инсульта и спонтанных желудочных кровотечений.
3. Симптомы заболевания
В симптоматике ИТП выделяют две разновидности болезни: сухая и влажная.
В первом случае наблюдаются только подкожные капиллярные кровоизлияния. При влажной тромбоцитопенической пурпуре возникают также наружные кровотечения из носа, слизистых. В обоих случаях кровотечение начинается без видимой причины. Чаще пятна появляются ночью, когда человек практически неподвижен и вероятность механических повреждений исключена. У больных идиопатической тромбоцитопенической пурпурой заболевание никак не влияет на внутренние органы. Температура тела нормальная, не увеличены лимфоузлы, отсутствуют симптомы интоксикации и воспаления.
Геморрагии на коже возникают преимущественно на передней поверхности тела, на лбу и конечностях. Никогда не бывает подкожных кровотечений на ладонях и подошвах. Наружные кровотечения – из носа, дёсен, миндалин, глаз, а также маточные и желудочные.
4. Диагностика и лечение
Диагностика ИТП основывается на тромбоцитопении, которую несложно выявить клиническим анализом крови или коагулограммой – анализом свертываемости. Сложнее (и важнее) дифференцировать это заболевание от иных болезней с тромбоцитопенической симптоматикой.
В период обострения ИТП наблюдается положительная реакция на ряд проб:
Лечение идиопатической тромбоцитопенической пурпуры чаще всего симптоматическое. При низких показателях свёртываемости крови больного госпитализируют. Показан постельный режим. При анемии и затяжных кровотечениях применяется соответствующая терапия. При снижении остроты состояния постепенно разрешается вставать и двигаться.
Обычно заболевание идиопатической тромбоцитопенической пурпурой рано или поздно заканчивается спонтанным самоизлечением или длительной ремиссией. Лишь в 1-2% случаев болезнь приводит к кровоизлиянию в мозг с летальным исходом, и именно поэтому вторичная профилактика включает снижение физической нагрузки, щадящий род деятельности, особое наблюдение при вакцинациях, оперативном лечении, стоматологических процедурах. Необходимо знать факторы, снижающие выработку тромбоцитов, и избегать их воздействия.
Идиопатическая тромбоцитопеническая пурпура: от Верльгофа до наших дней
Среди орфанных заболеваний, список которых в последние годы, по мере доступности генетического мониторинга, развития молекулярных и цитогенетических исследований, регулярно пополняется, идиопатическая тромбоцитопеническая пурпура (ИТП) имеет достаточно длинную историю изучения.
Спонтанное кожное кровотечение, известное более 2500 лет, уже тогда, в греческом и римском периоде врачевания, называлось «пурпурой». В 1735 году Паул Верльгоф (ИТП называют также «болезнью Верльгофа») описал 16-летнюю девочку с носовым кровотечением и кровотечением слизистых, которые купировались применением лимонной кислоты. Он назвал это заболевание «Morbus Maculosus Haemorhhagicus». Но заметного прогресса в лечении больных с ИТП достигли позже: в 1916 году в Праге профессор Шлоффер удалил селезенку у женщины с этим заболеванием. После операции последовало значительное увеличение числа тромбоцитов. И до сих пор спленэктомия является одним из вариантов лечения пациентов при ИТП. Однако наиболее полная картина этой патологии, наше представление о механизмах ее возникновения и подходах к диагностике и терапии начали складываться лишь в последнее время.
Идиопатическая тромбоцитопеническая пурпура (ИТП), или первичная иммунная тромбоцитопения (ИТП), является аутоиммунным приобретенным заболеванием, которое характеризуется изолированной тромбоцитопенией числом тромбоцитов ниже 100х10 9 /л. Оно может проявляться геморрагическим симптомом различной степени выраженности – от петехиальных кожных кровоизлияний до угрожающих жизни кровотечений. Болеют и дети, и взрослые. Этиология ИТП неизвестна. Поэтому и называется «идиопатическая». Среди пусковых факторов наибольшую группу составляют инфекции, беременность, а также прививки, стрессы.
Известно, что доминирующий механизм развития тромбоцитопении при ИТП обусловлен выработкой аутоантител к структурам мембраны тромбоцитов и их предшественников – мегакариоцитов, которые приводят к повышенному разрушению тромбоцитов фагоцитами, главным образом в селезенке, реже в печени, и недостаточной выработкой тромбоцитов в костном мозге. У пациентов с ИТП вырабатываются главным образом IgG аутоантитела против гликопротеинов GPIIb/IIIa или GPIb/IX поверхности тромбоцитов. Процесс формирования иммунной реакции на собственные тромбоциты – сложный, многоступенчатый, циклический. В нем принимают участие В-лимфоциты, Т-лимфоциты, NK-клетки, макрофаги. Помимо антителообразования, большую роль в патогенезе ИТП играют субпопуляции Т-лимфоцитов, развитие дисбаланса Т-клеточного звена иммунного ответа. Выявлена связь между ИТП и некоторыми генами-кандидатами, что указывает и на наличие генетической предрасположенности к ИТП.
С учетом сопутствующей патологии у пациента образуется определенный фенотип заболевания. Таким образом, патогенез ИТП связан с глубокими нарушениями иммунной системы. В связи с этим идиопатическая тромбоцитопеническая пурпура переименована на первичную иммунную тромбоцитопению с неизвестной этиологией. Соответственно, при всех других формах иммунная тромбоцитопения с известной этиологией будет симптомом других аутоиммунных заболеваний – системной красной волчанки (СКВ), антифосфолипидного синдрома (АФЛС), ревматоидного артрита (РА) и др.
В настоящее время продолжается поиск этиопатогенетических механизмов развития этой редкой патологии, которые могли бы стратифицировать пациентов на группы риска для индивидуализации лечебной тактики.
В литературе ИТП описывается как редкое, орфанное, заболевание. Надо сказать, что в медицинском мире не существует единого определения этой группы заболеваний. В одних странах орфанные патологии выделяют в зависимости от количества страдающих, в других – от доступности методов лечения, в третьих – к редким заболеваниям относят только хронические, угрожающие жизни.
Все эти законодательные решения привели к тому, что в ФГБУ «НМИЦ гематологии» в 2012 году было создано отделение – стационар орфанных заболеваний (руководитель: профессор Е.А. Лукина). Нозологический диапазон патологий, которыми занимается отделение, очень широк.
Лекарства, разработанные для лечения редких заболеваний, также называются орфанными препаратами и включены список дорогостоящих ЛС. Назначение орфанного статуса заболеваниям и любым лекарственным препаратам – социальный, политический вопрос во многих странах, как и в России. Поддержка исследований редких болезней со стороны правительств привела к прорывам в медицине, которые не могли бы быть достигнуты в рамках до этого существующей системы финансирования.
Статус орфанного заболевания для ИТП также открывал новые возможности для улучшения его диагностики и лечения современными методами, которые не могли бы быть осуществлены без него. Речь идет прежде всего о двух орфанных дорогостоящих препаратах агонистов тромбопоэтиновых рецепторов (аТПО) (ромиплостим от «Новартис» и элтромбопаг от «Амджен»). Лекарственное обеспечение осуществляется за счет бюджетов субъектов Российской Федерации.
Эпидемиология
Надо напомнить, что в нашей стране на популяционном уровне заболеваемость ИТП до 2014 года не была изучена. И информации для оценки особенности течения, эффективности и безопасности различных вариантов терапии больных ИТП было недостаточно. Для решения этих проблем под эгидой Национального гематологического общества (председатель Наблюдательного совета НГО – главный внештатный гематолог РФ, директор ФГБУ «НМИЦ гематологии» Минздрава России, академик РАН, профессор В.Г. Савченко) в начале декабря 2012 года был сформирован и начал функционировать «Регистр заболеваний системы крови». 3 С 2014 года стартовала работа и в его подразделе «ИТП» – началось многоцентровое проспективное наблюдательное когортное исследование «Эпидемиологические и клинические характеристики ИТП у взрослых в России» (руководитель: А.Л. Меликян).
Диагностика
Главным клиническим проявлением ИТП является геморрагический синдром, и прогноз течения заболевания всецело зависит от степени его тяжести. Риск развития кровотечений у больных с ИТП оценивается по количеству тромбоцитов в анализе периферической крови. Согласно данным регистра, в 70,0% случаев количество тромбоцитов в дебюте заболевания составляет от 3 до 30х10 9 /л, среди них у 35% выявляется критический уровень тромбоцитов (от 3 до 10х10 9 /л) с риском развития спонтанных настораживающих, жизнеугрожающих кровотечений, что требует незамедлительного назначения лечения.
Геморрагический синдром проявляется в виде: кожных геморрагий – 77% случаев; кровоточивости слизистых полости рта – 39%; носового кровотечения – 31%; менометроррагии – 15% (среди женщин); желудочно-кишечного кровотечения – 7%; гематурии – 4%; внутримозгового кровотечения – 0,9%, других – 1% (кровоизлияния в сетчатку глаз, геморроидального кровотечения ). 4
Таким образом, около 1/3 пациентов на момент постановки диагноза имеют геморрагические проявления, соответствующие тяжелой форме ИТП (3‒4-й степени кровоточивости по классификации ВОЗ). ИТП – заболевание не генетическое, но обычно сопровождает пациента на протяжении всей его жизни и является неизлечимым. Течение заболевания осложняется еще тем, что у 60‒70% пациентов через 12 месяцев (хроническая фаза) заболевание приобретает хронический, рецидивирующий характер, вновь.
ИТП – заболевание не генетическое, но обычно сопровождает пациента на протяжении всей его жизни и является неизлечимым. Течение заболевания осложняется еще тем, что у 60‒70% пациентов через 12 месяцев (хроническая фаза) заболевание приобретает хронический, рецидивирующий характер, вновь появляется геморрагический синдром, требующий проведения противорецидивного курса терапии.
Диагноз «ИТП» – это диагноз исключения, т.е. до настоящего времени нет ни одного специфического теста заболевания. Тромбоцитопении различного генеза регистрируются при широком спектре заболеваний гематологической, негематологической и врожденной природы, у которых длительное время доминирующим клиническим симптомом может быть изолированная тромбоцитопения. Поэтому для установления истинных причин тромбоцитопении необходимо проведение расширенного диагностического поиска в дебюте заболевания. 4
Первоначальный подход к диагностике причин тромбоцитопении основывается на анамнезе пациента (его фоновых заболеваниях и предшествующей медикаментозной терапии), его объективном физическом осмотре и обследовании по протоколу. Разработанный нами протокол дифференциального диагноза тромбоцитопений включен в Национальные клинические рекомендации по ИТП. 5 Самое главное, что все предложенные лабораторные и инструментальные исследования существуют в рутинной практике и их проведение обязательно для всех пациентов с подозрением на ИТП.
После исключения других причин тромбоцитопении диагноз ИТП устанавливается на основании следующих критериев:
Важно иметь в виду: нередко для быстрого купирования геморрагического синдрома пациентам без обследования по протоколу назначаются кортикостероиды, что смазывает истинную клиническую картину вторичных иммунных тромбоцитопений и влияет на истинные результаты иммунологических анализов. По данным нашего отделения, до 15‒20% случаев в динамике при повторном обследовании по протоколу диагноз ИТП заменяется на другой. Картина болезни может меняться с течением времени, в связи с этим необходимо постоянно обновлять данные о состоянии больного, дифференциальную диагностику проводить на каждом этапе наблюдения/терапии ИТП. Таким образом, очень важно дифференциальный диагноз проводить между первичной и вторичной тромбоцитопенией не только в дебюте заболевания, но и при рецидиве тромбоцитопении.
Установление истинных причин тромбоцитопении крайне важно для выбора адекватной терапии таких пациентов
Во многих случаях пациенты с первичной и вторичной ИТП получают аналогичное лечение. Тем не менее, если ИТП развивается на фоне основного заболевания (например, СКВ, АФС, HCV-инфекции, ВИЧ-инфекции или лимфопролиферативного заболевания), то лечение должно быть направлено главным образом на него.
Следует отметить, что осведомленность наших врачей об этом заболевании находится на достаточно высоком уровне. Во-первых, как выше сказано, ИТП описано 275 лет тому назад. Во-вторых, ИТП ‒ довольно распространенное среди редких заболевание. Ежегодно только в нашем отделении консультируются более 300 пациентов с диагнозом ИТП или с подозрением на нее. И наконец, впервые в России (в 2014 г.) разработаны Национальные клинические рекомендации (НКР) по диагностике и лечению идиопатической тромбоцитопенической пурпуры у взрослых наряду с другими нозологиями по инициативе Минздрава России. 4 Данные рекомендации постоянно обновляются и общедоступны. 4 Последняя редакция опубликована в 2018 году.
В 2019 году вышли обновленные клинические рекомендации Американской ассоциации гематологов (ASH) и обновленный Международный консенсус по диагностике и лечению первичной иммунной тромбоцитопении. Мы анализировали данные рекомендации и сравнивали с российскими клиническими рекомендациями по ИТП.
Хочу сказать, что глобальных изменений мы не заметили: особое внимание уделено правильной диагностике, а также более детально описаны подходы к лечению.
Кроме того, изучение ИТП входит в учебные и научные планы нашего Гематологического центра для гематологов, ординаторов, слушателей на циклах повышения квалификации ФГБУ «НМИЦ гематологии» Минздрава России и для специалистов других специальностей, поскольку имеются гематологические маски разных заболеваний. Наш Центр организует для врачей-специалистов стажировки на рабочем месте по актуальным вопросам гематологии как для гематологов, так и других специалистов. Все эти программы включены в систему непрерывного медицинского образования. В эру цифровизации и дистанционных образовательных технологий, проведения вебинаров, мастер-классов, обсуждения конкретных клинических примеров значительно расширяется аудитория обучающихся, что способствует непрерывному профессиональному росту врачей.
Лечение
Спленэктомия (СЭ), введенная в практику лечения еще в начале прошлого века Шлоффером, и сегодня является одним из вариантов лечения пациентов при ИТП. Она выполняется относительно часто, но в течение последних трех лет число таких вмешательств снизилась с 26 до 17%, при этом доля пациентов, получающих современные ЛС (агонисты тромбопоэтиновых рецепторов, аТПО) увеличилась с 5,9 до 45,7%. Такая же тенденция наблюдается и за рубежом, где частота выполнения спленэктомии меньше, чем в РФ.
С 1951 года в терапии заболевания используются кортикостероиды, до сих пор они остаются первой линией терапии пациентов с впервые диагностированной ИТП в зарубежных и российских протоколах – при геморрагическом синдроме и тромбоцитах менее 30‒50,0х10 9 /л или при отсутствии геморрагического синдрома при тромбоцитопении 9 /л.
Согласно данным нашего регистра, в 92,2% случаев в качестве первой линии пациенты получают лечение кортикостероидами как в виде стандартного лечения, так и пульс-терапии с эффективностью до 70‒80% с быстрым купированием геморрагического синдрома и повышением количества тромбоцитов выше безопасного уровня. Однако после отмены препарата быстро наступает рецидив заболевания. Кортикостероиды – эффективные средства, но с ними связано большое число потенциальных осложнений: сахарный диабет; тяжелые формы артериальной гипертензии и аритмий; язвенная болезнь ЖКТ, активные инфекции; психические расстройства. Поэтому повторные и частые курсы нежелательны. Во всех клинических рекомендациях строго ограничена продолжительность лечения кортикостероидами до 3‒4 недель. К сожалению, из-за доступности кортикостероиды назначаются и на последующих линиях терапии.
В 1980 году в университете при детской больнице в Берне 12-летнего мальчика с острой ИТП и иммунодефицитом лечили внутривенным иммуноглобулином (ВВИГ), что привело к заметному увеличению числа тромбоцитов в течение 24 часов. С тех пор ВВИГ широко и успешно применяется как в первой, так и в последующих линиях терапии в качестве «скорой помощи» в экстренных и жизнеугрожающих ситуациях и является совершенно неоценимым средством для лечения беременных с ИТП. ВВИГ в качестве первой линии терапии эффективен в 80% случаев, гемостатический эффект наступает на 1‒2-й день, длительность ответа – 1‒4 недели. Таким образом, фактически после первой линии терапии почти все пациенты – кандидаты второй линии терапии.
Для систематизации порядка назначения вариантов терапии международной рабочей группой по изучению ИТП выделены 3 стадии заболевания:
А последовательность назначения терапии при ИТП, разработанной на основании многолетнего клинического опыта, получила название линий терапии, которые в основном соответствуют стадиям заболевания.
В конце 2000 года, без сомнения, начинается новая эра лечения ИТП: препаратами современного поколения – стимуляторами тромбоцитопоэза, агонистами тромбопоэтиновых рецепторов, аТПО – ромиплостимом («Новартис») и элтромбопагом («Амджен»). В 2009 году они были одобрены в России как орфанные препараты для взрослых с рефрактерной хронической ИТП с/без спленэктомии. В 2015 году оба препарата включили в Перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения, утверждаемый распоряжением Правительства Российской Федерации. Использование аТПО (эти данные основаны на доказательной медицине и подкреплены несколькими основательными и очень качественными проспективными контрольными исследованиями) эффективно как до спленэктомии, так и после нее. С появлением данных препаратов прогноз заболевания улучшился, так как они предотвращают развитие тяжелых побочных эффектов лечения и позволяют добиться 80%-ного уровня непосредственного эффекта. 1,6
Я считаю (как и многие мои коллеги) их важными особенностями – органосохраняющий и кортикостероидсдерживающий эффекты.
В клинической практике сравнительно недавно появился еще один препарат для лечения ИТП – ритуксимаб, который разработан для лечения гематологических злокачественных заболеваний. В настоящее время ритуксимаб используется для лечения пациентов с ИТП, устойчивых к другим методам лечения. Его использование при хронической ИТП основывается на удалении аутореактивных В-лимфоцитов. Ритуксимаб включен в качестве 3-й линии терапии. Отмечается примерно 60%-ная вероятность получить первичный ответ. Но в России он не зарегистрирован для лечения ИТП, поэтому решение принимается индивидуально врачебной комиссией.
В 2018 году Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA) одобрило новый пероральный лекарственный препарат – селективный низкомолекулярный ингибитор селезеночной тирозинкиназы, фостаматиниб – для медицинского применения у пациентов с резистентной ИТП. А в 2019 – биодоступный агонист малой молекулы рецептора тромбопоэтина, аватромбопаг – для лечения взрослых пациентов с хронической ИТП, которые имели недостаточный ответ на предыдущую терапию. Оба препарата в России не зарегистрированы для лечения ИТП. Это перспектива.
При неуспешности разных вариантов терапии в последующих линиях терапии рекомендуется использование нереализующего метода или проведение комплексной терапии с использованием иммуносупрессоров.
Как правило, современные методы терапии все же позволяют достигнуть ремиссии различной длительности или состояния клинической компенсации. Но четкие прогностические критерии течения заболевания, ответа на терапию и исходов болезни до сих пор не разработаны – из-за природы и непредсказуемого течения заболевания.
Приступая к терапии хронической, рецидивирующей ИТП, необходимо помнить, что выбор терапии должен быть направлен на купирование кровотечения любой локализации, улучшение качества жизни больного, а не на нормализацию количества тромбоцитов любой ценой.
В клинической практике важно помнить, что терапию всегда следует подбирать индивидуально для конкретного пациента с учетом его возраста, коморбидности, сопутствующей патологии, а также учитывать предпочтения больного. Но наша практика часто сталкивается с объективными реалиями жизни.
По данным Е.Ю. Красильниковой (руководителя проектного офиса «Редкие (орфанные) болезни» Национального НИИ общественного здоровья им. Н.А. Семашко), при подготовке Ежегодного бюллетеня по редким (орфанным) заболеваниям 9 была получена информация от 76 регионов РФ, в которых на 1 января 2020 года проживало 3 860 пациентов с ИТП (из них 873 – дети), в лекарственной терапии нуждались 2069 человек (из них 468 – дети), получали лекарственную терапию 1 606 пациентов (из них 446 – дети). То есть патогенетическим лечением обеспечено 42% пациентов, внесенных в Федеральный регистр лиц, страдающих редкими жизнеугрожающими заболеваниями. 8
Фактически более половины пациентов не получают предназначенное орфанное лечение. Качество оказания медицинской помощи, которое включает диагностику, определение тактики терапии, коррекцию и контроль над этими показателями, стало возможным благодаря разработке схемы маршрутизации пациента, которая представляет путь больного от установления диагноза до обеспечения необходимыми лекарственными препаратами, то есть от лечащего врача до включения пациентов в список федерального регистра.
Наш опыт работы с региональными гематологами показывает, что все они хорошо осведомлены и соблюдают пути маршрутизации пациентов для получения орфанных лекарственных препаратов. В трудных ситуациях они обращаются в федеральные центры для получения решения врачебной комиссии по дорогостоящим препаратам. Обеспечение же в регионах только 42% пациентов с ИТП современными дорогостоящими орфанными ЛС главным образом связано с недостаточным финансированием в ряде регионах. И это тоже имеет свое объяснение. Число пациентов, нуждающихся в дорогостоящих орфанных препаратах, благодаря улучшению их диагностики увеличивается. Единственный выход – включение ИТП в федеральную программу финансирования высокозатратных нозологий.
Таким образом, идиопатическая тромбоцитопеническая пурпура (ИТП) – редкое (орфанное) хроническое, рецидивирующее заболевание, значительно ухудшающее здоровье и качество жизни больных по оценкам физического, социального функционирования, психического состояния. Кровотечения вызывают у них страх, тревожность и депрессию при кратковременном эффекте от проведенной терапии и побочных эффектах лекарств на фоне длительного лечения кортикостероидами, иммуносупрессорами.
ИТП полностью излечить нельзя, но можно эффективно сдерживать. Появившиеся в последние годы современные лекарственные препараты (агонисты тромбопоэтиновых рецепторов) при адекватном выборе дозы и контроля течения заболевания позволяют быстро купировать геморрагический синдром, достигать ремиссии различной длительности или состояния клинической компенсации, предотвращать развитие тяжелых побочных эффектов лечения, улучшать прогноз заболевания, что, естественно, не только повышает продолжительность жизни пациентов с орфанными заболеваниями, но и ее качество. Поэтому очень важно их включение в терапию всех пациентов, нуждающихся в ней. Сегодня эта равная доступность возможна лишь при включении ИТП в федеральную программу финансирования высокозатратных нозологий.