Синдром канавана что это такое
Болезнь Канавана
Проявляющееся в раннем детстве неврологическое заболевание, сопровождающееся нарушением моторики, гипотонией мышц, приступами эпилепсии, слепотой и макроцефалией, характеризующееся дефицитом фермента аспартоацилазы, называется спонгиозной дегенерацией, или болезнью Канавана.
По какой причине развивается болезнь Канавана?
Развитие патологии ведёт к демиелинизации нервных волокон головного мозга. Заболевание имеет генномутационную природу развития. Необходимо отметить, что данная патология относится к разряду редко встречаемых неврологических заболеваний. В подавляющем большинстве случаев заболевание развивается на первом году жизни ребёнка. К сожалению, приходится констатировать неутешительные результаты современных методов терапии. Неврологи относят патологию к разряду лейкодистрофии. Причиной развития патологии является мутация гена ASPA, который находится на семнадцатой хромосоме, отвечающего за выработку фермента аспартоацилазы, расщепляющего отдельные молекулы аспарагиновый кислоты, формирующейся в тканях нервной системы. Дефицит фермента неизбежно ведёт к переизбытку аспарагиновой кислоты, в следствие чего происходит разрушение миелиновой оболочки. Данный патологический процесс оставляет нервные клетки незащищенными и значительно ухудшает передачу нейронных импульсов. Болезнь Канавана относят к группе дегенеративных неврологических заболеваний.
В качестве основных симптомов болезни Канавана выделяют:
Как правило, к двухлетнему возрасту атрофируется зрительный нерв, что приводит к полной потере зрения.
Высокую концентрацию аспарагиновой кислоты позволяет установить общий анализ мочи. Для точной диагностики необходимо провести биохимический анализ крови, диагностику ДНК, магнитно-резонансную томографию. После подтверждения диагноза болезни Канавана невролог назначает симптоматическую терапию.
Как мы уже говорили выше, прогноз неутешительный. В большинстве случаев летальный исход наступает до достижения ребёнком десятилетнего возраста. Сегодня в специализированных клиниках проводят искусственную замену матированного гена на здоровый. Это позволяет значительно продлить жизнь больному, однако летальный исход неизбежен. Все, чего пока удалось добиться врачам в области лечения болезни Канавана — это увеличить продолжительность жизни больного до двадцати лет. На сегодняшний день отсутствует также специфическая профилактика данной патологии.
Синдром канавана что это такое
а) Терминология:
1. Сокращения:
• Болезнь Канавана (БК)
2. Синонимы:
• Спонгиоформная лейкодистрофия, спонгиозная дегенерация ЦНС, болезнь Канавана-ван-Богарта-Бертрана, недостаточность аспартазилазы, недостаточность ASPA, недостаточность ASP, недостаточность аминоацилазаы 2, недостаточность ACY2
3. Определение:
• Прогрессирующая аутосомно-рецессивная спонгиоформная лейкодистрофия
1. Общие характеристики болезни Канавана:
• Лучший диагностический критерий
о Мегалэнцефалия с диффузным ↑ сигнала от белого вещества на Т2-ВИ и ДВИ, а также ↑ пика NAA
• Локализация:
о Белое вещество (БВ): вовлечение в процесс субкортикальных U-волокон, сохранность внутренних капсул и мозолистого тела
о Таламусы, бледные шары (БШ), ± зубчатые ядра, сохранность хвостатых ядер и скорлупы
2. КТ признаки болезни Канавана:
• Бесконтрастная КТ:
о Диффузное ↓ плотности пораженных зон
3. МРТ признаки болезни Канавана:
• Т1-ВИ:
о Гипоинтенсивный сигнал от пораженных зон
• Т2-ВИ:
о Гиперинтенсивный сигнал от пораженных зон
• ДВИ:
о Гиперинтенсивный сигнал, ИКД от нормального до ↓ в пораженных зонах
• Постконтрастные Т1-ВИ:
о Контрастное усиление отсутствует
• МР-спектроскопия:
о ↑ NAA/Cr, ↓ Cho/Cr
4. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о МРТ
• Совет по протоколу исследования:
о Т2-ВИ, ДВИ и МР-спектроскопия
в) Дифференциальная диагностика болезни Канавана:
1. Болезнь «кленового сиропа»:
• ↑ аминокислот с разветвленной цепью + кетокислот
2. Болезнь Пелицеуса-Мерцбахера:
• ↑ ИКД, сохранность БШ и таламусов
3. Мерозиндефицитная врожденная мышечная дистрофия:
• ↑ ИКД, сохранность БШ и таламусов
4. Болезнь Александера:
• Характерно вовлечение БВ лобных долей, накопление контраста
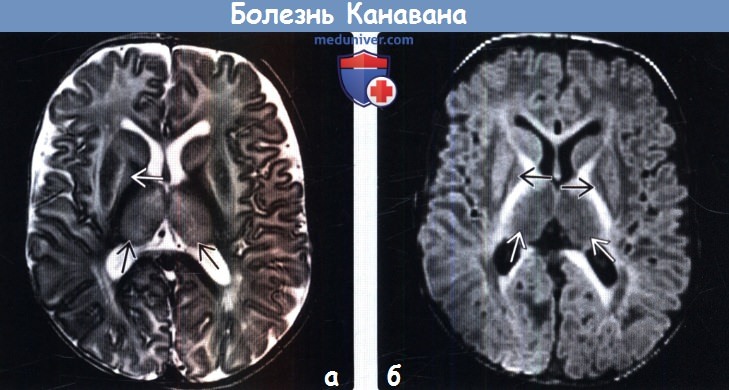
(б) МРТ, Т1-ВИ, аксиальный срез: у этого же шестимесячного ребенка отмечается диффузное снижение интенсивности сигнала от белого вещества, таламусов и бледных шаров. Внутренние капсулы, мозолистое тело, хвостатые ядра, а также скорлупа имеют нормальную интенсивность сигнала.
1. Общие характеристики болезни Канавана:
• Этиология:
о Недостаточность аспартоацилазы (которая метаболизирует N-a-цетиласпартат [NAA]) → ↑ ↑ NAA в головном мозге и моче
• Генетика:
о Аутосомно-рецессивный тип наследования → ген ASPA = длинное плечо 17-й хромосомы
2. Стадирование и классификация:
• Раннее начало → более быстрое прогрессирование
3. Макроскопические и хирургические особенности:
• Отек-набухание головного мозга
4. Микроскопия:
• Спонгиоформная дегенерация белого вещества; набухание астроцитов в БШ и таламусах
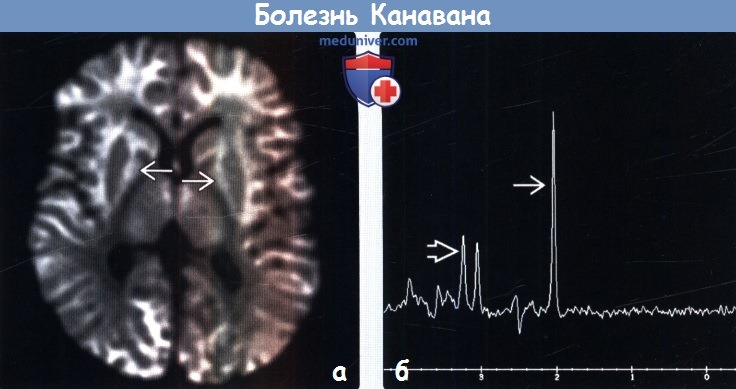
(б) Протонная МР-спектроскопия на томографе 1,5Т в аксиальной плоскости, длинное время эхо (ТЕ = 144 мс), область интереса в полуовальном центре: определяется выраженное относительное увеличение пика NAA и снижение пика холина по отношению к Cr для этого возраста.
г) Клиническая картина:
1. Проявления болезни Канавана:
• Наиболее частые признаки/симптомы:
о Три варианта клинического течения (в зависимости от возраста при постановке диагноза):
— Врожденный (первые несколько дней жизни):
Гипотония, быстрое наступление летального исхода
— Инфантильный (3-6 месяцев)
Наиболее частый вариант
Гипотония, запрокидывание головы, макроцефалия → судороги, мышечная спастичность, потеря зрения
— Ювенильный
о Дебют в возрасте 4-5 лет; наиболее медленно прогрессирующий вариант БК
• Клинический профиль:
о Раннее развитие тяжелой гипотонии и макроцефалия
2. Демография:
• Этническая принадлежность
о ↑ риск у евреев-ашкеназов (носительство в одном из 40 случаев)
3. Течение и прогноз:
• Неумолимо прогрессирующее нейродегенеративное заболевание: хроническое вегетативное состояние с вегетативными кризами → летальный исход к концу первой декады
4. Лечение:
• Методов лечения с доказанной эффективностью не существует (угнетение синтеза NAA путем нарушения работы гена Nat8l у мышиной модели)
д) Диагностическая памятка. Советы по интерпретации изображений:
• Отек-набухание головного мозга с ↑ интенсивности сигнала от белого вещества на Т2-ВИ и ДВИ, вовлечение БШ и таламусов
е) Список литературы:
1. Guo F et al: Ablating N-acetylaspartate prevents leukdystrophy in a Canavan disease model. Ann Neurol. 77(5):884-8, 2015
2. Baslow MH et al: Canavan disease, a rare early-onset human spongiform leukodystrophy: insights into its genesis and possible clinical interventions. Biochimie. 95(4):946-56, 2013
3. van der Knaap MS et al: Defining and categorizing leukoencephalopathies of unknown origin: MR imaging approach. Radiology. 213(1):121-33, 1999
— Вернуться в оглавление раздела «Лучевая медицина»
Редактор: Искандер Милевски. Дата публикации: 24.4.2019
Новости
Болезнь Канавана – грозный враг детей
Рождение ребенка – большая радость для отца и матери. Но иной раз, к сожалению, это событие оборачивается горем, когда становится ясно, что малыш поражен тяжелым и неизлечимым заболеванием. Одно из таких заболеваний – болезнь Канавана (или, точнее, «болезнь Канавана – ван Богерта»). Этот грозный недуг представляет собой наследственно-дегенеративное поражение нервной системы, приводящее к дистрофии белого вещества головного мозга. Как следствие – резкое ухудшение общего состояния и развития ребенка, нарушение моторики, трудности при глотании пищи, мышечная дистрофия. По мере прогрессирования болезни, возникают судороги, эпилептические припадки, ухудшается зрение (вплоть до слепоты). Заболевание довольно быстро приводит к смерти, способов излечения пока не найдено.
Вряд ли нужно объяснять, какая это беда не только для ребенка, но и для его родителей. Поэтому очень важно знать, из-за чего возникает такое заболевание, можно ли его предотвратить и что следует делать, если оно, к несчастью, диагностировано.
В чем причина возникновения болезни Канавана и как она диагностируется
Все вышеуказанные расстройства происходят вследствие генетической мутации, возникающей в 17-й хромосоме человека. Эта мутация приводит к хроническому недостатку в организме ребенка фермента аспартоацилазы, «отвечающей» за расщепление N-ацетил-аспарагиновой кислоты. Указанная кислота возникает естественным путем в процессе жизнедеятельности клеток центральной нервной системы. До тех пор, пока ее концентрация не превышает предельно допустимых величин, она не опасна, но патологически высокий уровень ее содержания в организме приводит к нарушению метаболизма липидов. А это, в свою очередь, вызывает разрушение оболочки нервных клеток (в значительной степени, состоящей из липидов). Нейроны, лишенные оболочки, теряют способность к нормальному функционированию и быстро погибают, со всеми вытекающими последствиями для организма.
Диагноз «болезнь Канавана» ставится ребенку неврологом по результатам анализа мочи на концентрацию N-ацетил-аспарагиновой кислоты. У больного наблюдается неестественно высокое содержание этого вещества (нередко до 20-кратного превышения нормы!) Анализ мочи проводится в большинстве случаев хроматографическим или масс-спектрометрическим методом.
Другие методы исследования, вплоть до МРТ и электроэнцефалографии, затруднительно производить, и к тому же они не дают должной эффективности ввиду малого возраста пациента.
Общие сведения об этом заболевании
Начиная с 19-го века, многие медики фиксировали факт неестественно высокого процента психических расстройств и младенческой смертности среди евреев ашкенази. Изучение этого факта по мере развития науки вообще и медицины в частности позволило Миртелю Канавану в 1931 году описать основные симптомы этого заболевания, получившего его имя. Разумеется, тогда еще не было известно о генетической мутации в 17-й хромосоме, поскольку генетика только начала развиваться и до открытия знаменитой «двойной спирали» было далеко.
А в 1987 году врач Рубен Маталон добился от семьи своих пациентов (где были две девочки с болезнью Канавана) согласия на предоставление их биологических материалов для исследований. Получив образцы тканей девочек, Маталон начал эксперименты с целью обнаружения гена, «ответственного» за развитие болезни, и через несколько лет его усилия увенчались блестящим успехом. (В источниках встречаются упоминания различных дат: 1991 или 1993 год). Впоследствии Маталон разработал тест, позволяющий определить риск развития болезни Канавана у плода во время беременности, что привело к конфликту с Фондом Канавана, который сам, в свою очередь, разработал аналогичный тест и бесплатно распространял его среди беременных. Споры и судебные тяжбы завершились подписанием компромиссного мирового соглашения.
Возникнуть это заболевание может у ребенка любой национальности, но до сих пор в особой «группе риска» находятся евреи ашкенази, поскольку среди них наибольшее число носителей больного гена: порядка одного человека из сорока (т.е. около 2,5%).
Болезнь Канавана
Болезнь Канавана — это генетическая аутосомно-рецессивная нейродегенеративная болезнь, известная также под названиями Болезнь Канавана-Ван Богерта-Бертрана. Это спонгиозная дегенерация белого вещества мозга, спонгиозная младенческая дегенерация, при которой наблюдается прогрессирующее поражение нервных клеток головного мозга. Аутосомно-рецессивный тип наследственности значит, что ребенок, родившийся от родителей-носителей данного заболевания, имеет высокий риск заболеть (примерно 25%). Это заболевание редкое, но в то же время одно из наиболее распространённых у детей, связанное с нарушением работы мозга. Принадлежит к группе генетических заболеваний под названием лейкодистрофия.
Проявляется болезнь в раннем детском возрасте, распространена в большей степени среди еврейского населения ашкенази.
Причины возникновения болезни Канавана
Болезнь Канавана вызывается мутировавшим геном ASРА, который синтезирует фермент аспартоацилазы и находится в семнадцатой хромосоме.
В головном мозге в высокой концентрации из аспаргиновой кислоты образуется ацетиласпарагиновая кислота и присутствует там так же, как и глутаминовая кислота.
Роль и значение этой кислоты до конца не определено, но известно, что недостаток аспартоациллазы приводит к возникновению болезни Канавана. Тогда эта кислота выводится из организма с мочой, повышая ее концентрацию в разы. Большое количество этой кислоты появляется в крови и самом головном мозге, особенно в белом веществе, где наблюдается резкое набухание астроцитов.
При электронной диагностике выявляется деформация митохондрии. В головном мозге происходят прогрессирующие атрофические процессы, в следствие которых увеличиваются в объеме мозговые желудочки. Нарушается образование миелиновой оболочки (особенный слой жиров, покрывающий нервные клетки как бы изолируя их, не позволяя нервному импульсу переходить из одного нервного волокна в другое).
Симптомы болезни Канавана
Болезнь Канавана изначально может никак не проявляться. Только спустя месяц или три месяца после рождения ребенка вероятно поставить окончательный диагноз.
К симптомам болезни Канавана относятся:
Симптомы болезни Канавана быстро прогрессируют, поэтому продолжительность жизни пациентов сокращается. Конечная стадия развития заболевания характеризуется обездвиживанием пациента, затруднительным дыханием и кровообращением.
Диагностика болезни Канавана
Диагностика болезни Канавана — сложный процесс, потому что похожие симптомы наблюдаются и среди других врожденных или приобретенных болезней.
Для определения болезни Канавана или подтверждения диагноза проводится тщательная диагностика, включающая в себя:
Анализ мочи и крови сразу выявляет высокую концентрацию ацетиласпарагиновой кислоты. Процесс проведения МРТ затруднителен, так как возраст пациентов очень мал, поэтому могут возникать неточности в диагностике. МРТ помогает выявить губчатую дегенерацию нервных волокон миелинового жирового слоя, а также набухание астроцитов и деформацию (удлинение) митохондрий. Концентрация аспартоацилазы в кожных фибробластах у носителей болезни Канавана приблизительно в два раза ниже нормы. Магнитно-резонансная спектроскопия показывает наивысшую концентрацию ацетиласпарагиновой кислоты в головном мозге. Особенно важен биохимический анализ крови и мочи, которые и дают заключение диагноза, играют решающую роль.
Существуют методы диагностики, позволяющие выявить данное заболевание ребенка еще в утробе матери (перинатальная диагностика). Для этого нужно установить в первую очередь деформированный патологический ген у обоих родителей. Для подтверждения или опровержения диагноза проводится амниоцентез для получения амниотической жидкости. Практикуют также трансабдоминальную или трансцервикальную биопсию хориона для получения ворсины хориона.
Генетики рекомендуют лицам, имеющим в семейной истории данное заболевание, при планировании семьи проходить тщательное обследование — скрининг на выявление модифицированного гена.
Лечение болезни Канавана
Эффективной и стандартной методики, как и лекарств для лечения болезни Канавана, на сегодняшний день не существует. Курс лечения сугубо индивидуален и имеет поддерживающий характер. Болезнь считается смертельной. Пациенты умирают зачастую в возрасте до двух лет, в отдельных случаях продолжительность жизни может быть до десяти лет, в редких случаях до двадцати. С помощью метаболической терапии возможно замедление развития болезни. Прием ряда медицинских препаратов (ацетат кальция, цитрат лития, сукцинат натрия, милидиамокс) сможет приостановить прогрессирование заболевания, но остановить его не сможет. Все препараты, необходимые для лечения — дорогостоящие.
Экспериментальное лечение
Эксперименты медиальной терапии на основе нитрата лития (проводились в лабораторных условиях на организмах животных) дали обнадёживающие результаты приостановления заболевания. Это стало основой для продолжения экспериментального лечения на основе лития.
На уровне экспериментов исследуются разнообразные методы лечения, в частности, генная терапия. Например, в желудочки мозга пациента через несколько катетеров были введены липосомы с геном аспартоациалазы в качестве раствора. Процедура проводилась как экспериментальное лечение с участием более десятка больных детей и не привела к желаемому результату — полное устранение болезни, хотя и считается наиболее успешной, так как с ее помощью удалось приостановить развитие заболевания.
Обнадёживающие результаты дали эксперименты с использованием триацетина, который расщепляют до ацетата для лучшего усвоения организмом.
Прогноз болезни Канавана
Болезнь Канавана приводит к смерти пациента зачатую в первые два года развития, если не начать ее вовремя лечить. Применение генной терапии может продлить жизнь пациента на несколько лет. Зарегистрированы случаи прекращения болезни на непродолжительное время вследствие лечения генной терапией.
Синдром канавана что это такое
Это редкое генетическое заболевание, относится к группе лейкодистрофий, характеризующееся губчатой дегенерацией белого вещества мозга. При рождении дети с этой патологией могут выглядеть абсолютно здоровыми, так как обычно симптомы развиваются в возрасте 3-6 месяцев. Симптомы могут включать аномально большие размеры головы (макроцефалия), снижение мышечного тонуса, приводящее к «вялости», и задержку психо-речевого развития.
Белое вещество – это ткань головного мозга которая в основном состоит из миелинизированных аксонов, которые представляют собой длинные ретрансляторы, выходящие из сомы, и которые имеют белый цвет из-за относительно высокого содержания липидного жира в миелиновом белке, который их покрывает. Миелин имеется и в центральной, и в периферической нервных системах. В ЦНС он находится преимущественно в белом веществе (хотя некоторые его количества имеются и в сером), как раз придавая ему такой цвет. Миелин, который можно назвать миелиновой оболочкой, защищает нервные волокна, действует как изолятор и увеличивает скорость передачи нервных сигналов. Каждый тип лейкодистрофии поражает разные части миелиновой оболочки, вызывая ряд различных неврологических проблем.
История
Болезнь Канавана впервые была описана в 1931 году Миртеллой Канаван. В 1931 году она стала соавтором статьи, в которой обсуждалась ситуация с ребенком, который умер в возрасте 16 месяцев. Канаван была первой, кто идентифицировал это дегенеративное заболевание центральной нервной системы, которое позже было названо «болезнью Канавана».
Эпидемиология
Заболевание зарегистрировано во всем мире, но чаще встречается среди еврейского населения ашкенази. Заболеваемость тяжелой формой среди нееврейского населения оценивается примерно в 1: 100 000 новорожденных. Если оба родителя имеют еврейское происхождение ашкенази, частота составляет от 1: 6 400 до 1: 13 500 новорожденных.
Симптомы
Клинические проявления и прогрессирование болезни Канавана сильно варьируются. Дебют обычно происходит в возрасте от 3 до 6 месяцев, и начальные симптомы обычно включают плохой контроль движения головы, аномально большую голову (макроцепафалия) и сильно сниженный мышечный тонус (гипотония), приводящий к «вялости». Некоторые младенцы могут испытывать затруднения при глотании (дисфагия), что усугубляет трудности с кормлением. На этом фоне так же также наблюдается задержка в достижении основных этапов развития (например, дети не могут сидеть или стоять без посторонней помощи), и в большинстве случаев они никогда не ходят самостоятельно.
Дополнительные симптомы, которые поражают детей с болезнью Канавана, включают судороги, нарушения сна, трудности с кормлением, контрактуры крупных суставов, носовую регургитацию, гастроэзофагальный рефлюкс, и атрофию зрительных нервов что приводит к слепоте. В большинстве случаев это не влияет на слух, но могут и поражаться нервные волокна отвественные за слух. В последние несколько лет была выявлена легкая форма болезни Канавана с типичными мутациями в гене ASPA и при этом незначительным увеличением NAA в моче. Эти дети имеют негрубую задержку психоречевого развития, однако они могут учиться и ходить в школу. Голова может быть несколько увеличена, но типичные изменения белого вещества, связанные с болезнью Канавана, могут отсутствовать. Прогноз, безусловно, намного лучше, чем при класической форме.
Генетические особенности
Это аутосомно-рецессивное заболевание, вызванное мутацией гена на коротком плече 17й хромосомы. Ген ASPA синетзирует фермент аспартоацилаза. Этот фермент расщепляет N-ацетиласпартат (NAA), который находится в нейронах головного мозга. Функция NAA неясна. Изначально предпологали что он играет роль в производстве миелиновой оболочки, но недавние исследования показывают, что NAA не имеет этой функции. Вместо этого фермент может участвовать в транспортировке молекул воды из нейронов. Мутации в гене ASPA снижают функцию аспартоацилазы, которая предотвращает нормальный распад NAA. Если NAA не расщепляется должным образом, возникающий в результате химический дисбаланс мешает формированию миелиновой оболочки по мере развития нервной системы. Накопление NAA также приводит к прогрессивному разрушению существующих миелиновых оболочек, что нарушает нормальное развитие мозга.
Дифференциальная диагностика
Терапия
На данный момент нет ни одного зарегистрированного препарата от болезни Канавана. Лечение носит симптоматический поддерживающий характер. Физическая терапия может помочь улучшить моторику, а образовательные программы могут помочь улучшить коммуникативные навыки. Приступы лечат противоэпилептическими препаратами, а гастростомия используется для поддержания адекватного приема пищи и гидратации при наличии проблем с глотанием. Продолжительность жизни варьрируется в зависимости от тяжести состояния и не превышает 10 лет жизни.
Клинический случай
В начале 2021 года к нам к клинику поступил мальчик в возрасте 4 месяцев, с основными жалобами при поступлении: ежедневные серийные судорожные приступы, грубая задержка психомоторного развития, отсутствие пищевого поведения, комплекса оживления, снижение массы тела.
Анамнез заболевания: ребенок от 2 беременности (сестра 2,5 года – здорова), с ОРВИ в 20 недель, носительство коронавирусной инфекции в 38 нед. Роды путем планового кесарева сечения в 38 недель. При рождении масса 2770гр, длина 52 см, Апгар 8/9 баллов. Выписан из роддома на 17 с/ж в связи с перинатальным контактом по COVID. По данным НСГ определялись постгипоксичесике (?) Изменения. В 1 месяц осмотрен неврологом – перинатальное поражение ЦНС с нервно-рефлекторной возбудимостью.
В 2 месяца – окружность головы +10 см от рождения, однако по НСГ признаков повышения внутричерепного давления не отмечалось.
Проведено КТ головного мозга по месту жительства – признаки перивентрикулярной лейкомаляции.
Так же по месту жительства проведено МРТ головного мозга где были выявлены признаки лейкодистрофии.
Исключен синдром Ван дер Кнаап молекулярно-генетическим методом.
Данные объективного осмотра: Состояние пациента тяжелое. В сознании. Ребенок не контактен. Положение вынужденное. Вес/масса тела: 7 кг. (перцентиль 50-75%). Индекс массы тела: 16,57. Рост/длина: 65 см. (перцентиль 90-97%). Площадь поверхности тела: 0,36 кв.м. Окружность головы: 45 см. (перцентиль> 97%). Окружность груди: 44 см. (перцентиль 75-90%). Физическое развитие: очень высокое. Тип телосложения гармоничный. Имеются единичные микроаномалии. Кожа: сухая, на щеках – мелкоточечная сыпь. Слизистые оболочки не изменены. Подкожно-жировая клетчатка развита удовлетворительно. Лимфатические узлы множественные, мелкие, эластичные, безболезненные. Мышечная система развита удовлетворительно. Тонус мышц: нормальный. Форма грудной клетки правильная. Костные деформации не выявлены. Утолщение ногтевых фаланг пальцев нет. Суставы не изменены. Частота дыхания: 32 в мин. Одышки нет. Носовое дыхание свободное. Голос не изменен. Кашель не отмечается. Мокроты нет. Кровохарканье нет. Перкуторный звук не изменен. Дыхание: жесткое. Хрипы не слышны. Пульс: 120 в мининуту, ритм правильный. А/Д (прав.рука): 85/55 мм.рт.ст. Пульс на лучевых артериях нормальный. Перкуссия сердца границы соответствует возрасту верхняя – не изменена правая – не изменена левая – не изменена. Тоны сердца: отчетливые, ритмичные, выслушивается шум. Фаза сердечного цикла: систолическая. Аппетит: удовлетворительный, принимает противосудорожную тепатию. Тошноты нет. Рвоты нет. Другие диспептические явления не выявлены. Язык: чистый. Склеры: не изменены. Живот: мягкий, безболезненный. Симптомы желчного пузыря: отрицательные. Точки проекции поджелудочной железы: безболезненные. Асцита нет. Печень пальпируется. Край закруглен, эластичный. Селезенка: не пальпируется. Симптомы раздражения брюшины: нет. Стул не изменен. Мочеиспускание безболезненное. Дизурические явления не выявлены. Симптом поколачивания отрицательный. Вторичные половые признаки соответствуют возрасту. Осмотр половых органов сформированы правильно по мужскому типу. Психическое развитие: грубая задержка психо-речевого развития. Черепные нервы: Реакция зрачков на свет живая, зрачки симметричны. Глазные щели симметричны. За предметом не прослеживает, взгляд фиксирует кратковременно.
Сосание, глотание присутствуют, периодически поперхивается пищей. Корнеальный рефлекс вызывается. Лицо в покое и при плаче симметрично, мимика скудная. Мягкое небо симметрично, глоточный рефлекс живой. Язык в полости по средней линии, Кривошеи нет. Общая двигательная активность снижена.
Положение рук и ног свободное. Пронация и супинация кистей рук полная. Тонус мышц в руках в норме D=S. Тонус мышц в ногах в норме. D=S. Сухожильные рефлексы оживлены. При осмотре отмечаются серийные симметричные спазмы, миоклонии левых конечностей с заведением глаз с предшествующей икотой.
На момент госпитализации: Дебют эпилепсии – отведение глаз вправо, клонические подергивания в руках. На этом фоне была назначена противосудорожная терапия, с положительной динамикой в виде снижения числа приступов.
При видео ЭЭГ мониторинге выявлена диффузная эпилептиформная активность в виде одиночных комплексов острая-медленная волна амплитудой до 120 мкв.
По данным лабораторных исследований, Общего клинического анализа крови, исследования показателей основного обмена, биохимического исследования крови, значимых изменений показателей не выявлено.
Сердечно сосудистая система без патологических изменений.
Врач-офтальмолог – косоглазие расходящееся непостоянное.
На МРТ головного мозга – Отмечается диффузное поражение белого вещества больших полушарий головного мозга. Имеет место ограничение диффузии в пораженном белом веществе. На этом фоне отмечается уменьшение объема серого вещества. Базальные ядра несколько увеличены, вблизи чечевицеобразных ядер с обеих сторон визуализируются небольших размеров ликворные кисты. Очаговых изменений в стволе и мозжечке не выявлено. Срединные структуры головного мозга не смещены. Мозолистое тело истончено на всем протяжении. Ликворная система не изменена.
