Секвенирование что это в генетике
Секвенирование что это в генетике
Сегодня много пациентов страдает от неверного диагноза или несвоевременно обнаруженного заболевания, связанного с нарушениями в структуре ДНК.
Распространенные генетические тесты, такие как анализ одного гена, панели из нескольких генов или микроматричный анализ, часто не могут до конца выявить точную причину болезни из-за своих ограниченных возможностей.
Недавние достижения молекулярной генетики позволили сделать доступным по цене и скорости выполнения новый метод генетического тестирования — полногеномное секвенирование.
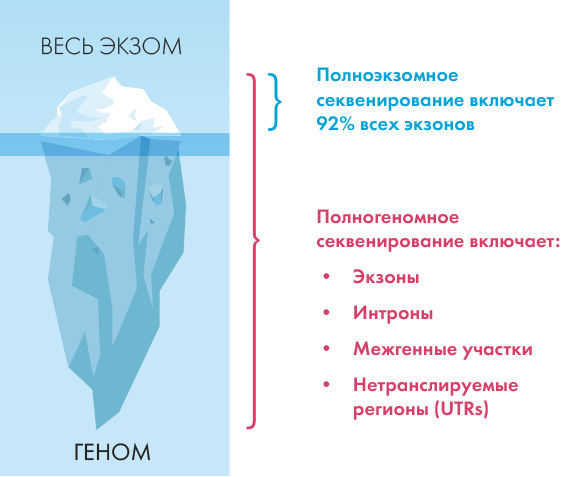
Полное секвенирование генома способно обнаружить почти все изменения в ДНК пациента, расшифровывая последовательность всех кодирующих и некодирующих областей. Результат такого исследования — информация о тысячах генов, участвующих в нормальном росте и развитии организма.
Этот метод с успехом заменяет все ранее известные способы генетического тестирования, соединяя в себе их возможности. С каждым годом он позволяет установить точный диагноз все большего числа заболеваний.
Используя полногеномное секвенирование, лечащий врач получает помощь не только в диагностике, но и более точно принимает решения по лечению, может наблюдать за течением заболевания, делать прогноз развития болезни и выздоровления. Точные рекомендации о прогрессировании заболевания также возможны в некоторых случаях.
По результатам тестирования может быть проведена оценка риска наследственных заболеваний для других членов семьи.
Полное секвенирование может быть проведено по направлению лечащего врача, а также по желанию пациента без наличия срочных медицинских показаний.
Структура генома не изменяется в течение всей жизни. Сделав анализ однократно, его результатами можно пользоваться всю жизнь. К ним можно повторно обращаться при появлении очередных открытий в генетике и с учетом новых знаний более точно интерпретировать данные.
Имея на руках готовую расшифровку своего генотипа, человек подготовит себя к возможным экстренным ситуациям, когда подробная генетическая информация может спасти жизнь — травмы, операции, тяжелые заболевания, пересадка органов и другие.
Полногеномное секвенирование — лучший на сегодня метод продолжать исследование структуры ДНК, функций генов, их влияния друг на друга и на проявления фенотипа.
Хотя крупные исследовательские центры в мире ведут эту работу, ее результаты не всегда широко доступны.
Поэтому многие исследователи делают это самостоятельно для своих узкоспециализированных целей — подбор и разработка препаратов, спортивные достижения, селекция растений и животных, диагностика и лечение болезней.
Лаборатория «Геномед», обладая современным оборудованием, проверенными технологиями и квалифицированными специалистами-генетиками, готова предоставлять эти ресурсы для целого ряда научных разработок.
Фундаментальные исследования
Изучение структуры и функции генома
Исследование генома человека не завершено до сих пор. Полногеномное сенквенирование дает новые возможности поиска нераскрытых функций генов, изучения некодирующих областей и регуляторных участков ДНК.
Структурные изменения и CNV
В отличие от большинства других генетических методов полногеномное секвенирование позволяет точно определять любые изменения структуры ДНК.
Часто достигается точность определения до уровня единичного нуклеотида. Поэтому, если требуется достоверно определить транслокации, инверсии, вставки или делеции участков, стоит использовать тест Genome UNI.
Эпигенетика
После создания технологии полногеномного секвенирования появилась возможность изучать закономерности наследования, не связанные с генетической последовательностью. В первую очередь речь идет о механизмах регуляции экспрессии генов.
В вопросах эпигенетики важную роль играют методики исследования метилирования ДНК (MeDIP-Seq, WGBS), взаимодействия и модификации гистонов (ChlP-Seq), метилирования РНК (TRM).
Полногеномные ассоциативные исследования
Исследование связи между структурой генома и фенотипическими признаками позволяет выявить, как проявляются различные сочетания генов.
Результат такой работы — более четкое понимание механизмов развития полигенных и многофакторных заболеваний, выявление влияния гетерозиготности на развитие признаков и оценка влияния средовых факторов.
Митохондриальный геном
В отличие от других генетических тестов полногеномное секвенирование исследует одновременно весь генетический материал клетки — ДНК ядра и ДНК митохондрий. Это особенно важно при изучении наследственности по материнской линии и обнаружении наследственных митохондриальных заболеваний.
Транскриптом
Полногеномное секвенирование позволяет оценивать не только геном клетки, но и ее транскриптом — совокупность всех типов РНК.
Важность транскриптома в том, что он показывает активность экспрессии определенных генов на текущий момент. Эта активность сильно зависит от состояния окружающей среды и самого организма и может говорить о наличии неблагоприятных процессов.
Биоинформатический анализ
Расширенный пайплайн
Многопотоковое секвенирование позволяет одновременно проводить расшифровку множества участков одной ДНК. Это значительно ускоряет процесс чтения, позволяет снизить стоимость и добиться высокой точности.
В настоящее время полногеномный анализ покрывает больше 96% генов с глубиной прочтения >20х, а время исследования одного генома сократилось до 1 суток.
Платформа управления данными
Результаты анализов представлены в виде удобного пользовательского интерфейса в личном кабинете. Там же доступны данные интерпретации, если она проводилась, и полученные рекомендации.
Владелец доступа может в любое время обратиться к своим результатам или загрузить их для off-line использования.
Пользовательский биоинформационный сервис
Кроме оборудования и передовых технологий «Геномед» рад предоставить консультационные услуги опытных врачей-генетиков.
Направляя пациента на анализ, вы получите не только расшифровку нуклеотидной последовательности, но и, при необходимости, ее клиническую интерпретацию и рекомендации по использованию результатов.
Собственное хранилище данных
Данные о проведенных исследованиях хранятся на собственных серверах лаборатории.
Все данные шифруются и доступ к ним предоставляется исключительно заказчику с индивидуальным логином и паролем.
Прикладные исследования
Диагностика генетических заболеваний
Сегодня насчитывают около 6000 различных генетических заболеваний и нарушений. Многие из них обладают схожими симптомами, но вызваны патологией разных генов. Если искать эти заболевания по отдельности, потребуется огромное количество исследований.
Полногеномное секвенирование позволяет заменить все виды генетических и многих лабораторных исследований единственным точным и высокоинформативным тестом.
Геном опухоли
Полногеномное секвенирование опухоли дает ключ к пониманию канцерогенеза. Это не только определение основных мутаций, приводящих к развитию рака.
Получив полную расшифровку генома, онколог может оценить уровень сопротивляемости организма росту опухоли, следить за изменением опухоли под воздействием терапии, подбирать наиболее эффективные и безопасные сочетания препаратов.
Профилактическое здоровье
Данные об индивидуальных предрасположенностях к заболеваниям могут изменить образ жизни человека.
На этом основании проще подобрать диету, нагрузки, препятствовать или способствовать воздействию различных факторов внешней среды.
Это позволит не просто увеличить продолжительность жизни, но и улучшить ее качество.
Создание лекарств
Данные об индивидуальных предрасположенностях к заболеваниям могут изменить образ жизни человека.
В зависимости от своего генетического статуса человек по разному реагирует на лекарственную терапию. Гены влияют как на эффективность, так и на переносимость препаратов. Полногеномное тестирование позволяет решать две важные задачи фармакотерапии.
Первая задача — поиск биомаркеров заболеваний. Наглядный пример — простатоспецифический антиген, используемый для диагностики опухолей предстательной железы.
Вторая задача — персонализация лекарственной терапии. В идеале препарат должен разрабатываться для генотипически близких групп пациентов или даже индивидуально с учетом конкретного набора генов.
Судебная медицина / Судебная патология
Генетические данные сегодня широко используются в криминалистической и судебной практике. Ниже перечислены некоторые примеры такого применения. Определение родства\материнства\отцовства.
Антропология и этнос
Изучение ДНК предков или представителей различных этнических групп позволяет понимать историю происхождения и развития человека и законы передачи наследственной информации.
Для отдельного человека появляется возможность разобраться в своих корнях и родословной. Для общества и науки — это источник изучения этнических особенностей здоровья, заболеваемости, долголетия и возможностей развития.
Диагностика наследственных заболеваний
Анализ всего генома в одном исследовании чаще всего приводит к более быстрой постановке диагноза генетического состояния по сравнению с многочисленными сериями одиночных генетических тестов. Особенно это справедливо, если клиническая картина не дает генетику четких указаний, в каких локализациях следует искать патологию, либо тогда, когда клиника может быть обусловлена патологией разных или нескольких генов.
Репродуктивное здоровье
Четко определена связь ряда генов с репродуктивной функцией. Мужское и женское бесплодие, невынашивание, хромосомные болезни новорожденных — все эти состояния можно обнаружить, а впоследствии и успешно лечить, если знать состояние генов, ответственных за процессы зачатия и развития плода.
Онкология
Молекулярно-генетические исследования — мощный инструмент в борьбе с онкологическими заболеваниями.
Во-первых, расшифровав полный геном, можно оценить не только гены, напрямую связанные с развитием рака. Одновременно врач получает полную картину состояния антиоксидантной защиты, противоопухолевого иммунитета, антитоксической функции и других систем, которые косвенно влияют на появление и течение онкопроцесса.
Во-вторых, генетические методы позволяют более эффективно подобрать препарат, контролировать процесс лечения и склонность к рецидивированию.
Важно, что полногеномное исследование (WGS) экономически намного выгоднее, чем исследование отдельных генов или серии генетических панелей (наборов анализов генов, связанных с определенной патологией).
Сегодня с помощью полногеномного тестирования можно оценить 649 опухолевых генов и еще 28 генов, способных нести хромосомные транслокации (перенос участков ДНК между хромосомами), связанные с развитием рака.
Планирование семьи
Известно, что предрасположенность к заболеваниям передается по наследству. Существует группа заболеваний, которые зависят от состояния генов и носят название аутосомно-рецессивных.
Полногеномное секвенирование способно показать людям, вступающим в брак, риски рождения у них детей с аутосомно-рецессивными болезнями.
Предрасположенность к заболеваниям
Почему одни люди заболевают раком, а другие нет? Кто-то живет до 100 лет, многие же умирают в молодости. Как узнать причину?
Сегодня уже четко установлена связь многих генов с развитием заболеваний. Причем, состояние одних генов улучшает прогноз, других — ухудшает. Примеры таких болезней — атеросклероз, остеопороз, тромбозы.
Если знать сочетание всех генов, можно рассчитывать риск развития заболеваний для человека, даже если он пока абсолютно здоров, а также предотвращать их появление.
Индивидуальные способности
Для многих способностей и склонностей человека показана прямая зависимость от состояния его генотипа. К ним относятся мышечная выносливость и сила, темперамент, наклонность к разного рода зависимостям и многое другое. Если планировать профессию и образ жизни на основании генетического анализа, можно достигать лучших результатов быстрее и с меньшими усилиями.
Почему нужно использовать
секвенирование генома
Полногеномное тестирование обладает целым рядом преимуществперед другими методами
в скорости, широте и точности расшифровки генетической последовательности
и установлении диагноза.
| Секвенирование панелей генов | Клиническое секвенирование экзома | Полное секвенирование экзома | Genome UNI | |
|---|---|---|---|---|
| Покрытие кодирующих участков генома | Равномерное, только в области экзонов исследуемых генов | Неравномерное | Неравномерное | Равномерное по всему геному |
| Поиск вариантов в интронах | — | — | — | + |
| Поиск вариантов мтДНК | — | — | — | + |
| Определение CNVs с высокой точностью | — | — | — | + |
| Определение экспансии тринуклеотидных повторов | — | — | — | + |
| Вероятность выявления причины заболевания при повторном анализе данных | Низкая | Низкая | Средняя | Высокая |
| Показания к исследованию | Заболевания с преимущественным поражением одной системы органов или одним ведущим симптомом, когда определены гены ассоциированные с фенотипом | Подозрение на определенную генетическую патологию, когда другие методы (анализ отдельного гена или панели) недоступны | Секвенирование пробанда или родителей (трио) для поиска генов кандидатов (GUS) при отсутствии патогенных вариантов в клинически значимых генах | «В качестве теста первой линии у пациентов с признаками наследственного заболевания или при отсутствии специфического фенотипа.» |
| Другие особенности | Повышенное покрытие таргетных участков генома позволяет лучше выявить однонуклиотидные и in/del варианты | Нет рекомендованного перечня клинически значимых генов | Не обладает преимуществами при секвенировании только пробанда | Большой объем данных требует использования дополнительных вычислительных ресурсов |
Информация для исследователей
Фундаментальные исследования
Секвенирование и ресеквенирование генома, анализ метагенома, экспрессии и метилирования генов.
Прикладные исследования
Поиск биомаркеров, рекрутинг пациентов, решения для селекции.
Медицинские исследования
Секвенирование генома и экзома, анализ на микрочипах.
Биоинформатический анализ
Расширенный пайплайн, биоинформационный сервис, платформа управления данными, хранилище данных.
Genome UNI рекомендован:
Врачам на заметку!
Genome UNI выявит:
Обладает ли тест Genome UNI
доказанной эффективностью?
Для анализа данных используется проприетарный алгоритм и пайплайн, разработанный одной из ведущих компаний США, которая специализируется на анализе данных полного секвенирования генома.
Пайплайн разработан в соответствии с требованиями профессиональной ассоциации медицинских генетиков (ACMG) и ассоциации клинических патологов (CAP) США и включает возможность анализа данных с учетом формализованного описания фенотипа в терминах HPO.
Строгий подход к оценке качества лабораторных данных при использовании профессионального пайплайна позволяет не только повысить выявляемость вариантов, но и избежать ошибок которые могут возникнуть на стадии сиквенса и снизить вероятность ложноположительных результатов.
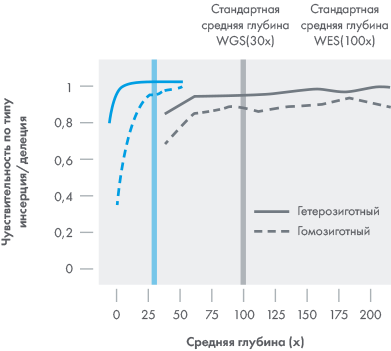
WGS выявляет больше инсерцционно-
делеционных вариантов при 30х чем WES
при средней глубине 100х
WGS охватывает больше генов на при 30х,
чем WES при 100х
КЛИНИЧЕСКОЕ СЕКВЕНИРОВАНИЕ
Самый современный метод диагностики наследственных заболеваний.
Точные методы диагностики:
Что такое секвенирование
Секвенирование — это метод определения нуклеотидной последовательности ДНК и РНК. Тестирование используется для определения генетических повреждений (мутаций) в ДНК, которые являются причиной наследственных болезней, наследственных предрасположенностей или особенностей организма. Существует несколько разновидностей секвенирования, которые позволяют выявлять возможные генетические отклонения и редкие генетические варианты, тонко влияющие на появление определенных патологий в человеческом организме.
Показания к проведению анализа с помощью метода секвенирования:
Для получения более подробной информации об исследовании вы можете позвонить по телефону:
либо воспользоваться консультацией врача-генетика
Основные этапы исследованияя
Вне зависимости от типа секвенирования процедура делится на несколько основных этапов:
Таргетное секвенирование
Возможности таргетного секвенирования
Метод таргетного секвенирования позволяет выделять и исследовать конкретные области геномов или отдельные гены. Технологии нового поколения позволяют рассчитывать время и затраты на исследование. Таргетному анализу могут подвергаться отдельные интересующие пациента гены, участки генов и митохондриальные ДНК.
Преимущества таргетного секвенирования
По сравнению с комплексными методами анализа таргетное секвенирование более выгодно. Исследуются лишь отдельные участки генов, в которых могут определяться мутации. В таком случае для диагностики требуется меньше ресурсов, поэтому таргетный поиск отдельных отклонений обойдётся гораздо дешевле, нежели полная диагностика.
Панели генов
Таргетные панели были разработаны в отношении групп заболеваний, объединенных какими-то общими симптомами, например, аутизм, задержка психического развития, онкологические заболевания и т.д. К примеру, если в истории семьи обнаруживаются признаки одного или нескольких различных наследственных опухолевых заболеваний, то семья вполне может быть носителем опухолевого наследственного заболевания. Панель “наследственный рак” объединяет серию генетических мутаций, которые могут приводить к наследственному раку. В некоторых случаях наиболее эффективной может оказаться первоначальная проверка при помощи таргетных панелей нового поколения, таких как CancerNext, с целью добиться полного покрытия задействованных генов.
Мультигенные панели
Группа исследований, предназначенных для диагностики клинически сходных заболеваний. Такие исследования могут включать от 10 до 600 генов. Они могут быть эффективны для уточнения диагноза, дифференциальной диагностики и поиска патогенных мутаций.
Полногеномный анализ
Полногеномное секвенирование дает максимально полный набор данных о структуре генетического материала и позволяет детально оценить все индивидуальные генетические вариации. Секвенатор нового поколения IlluminaNextSeq 500 может определять полную структуру генома человека за 2 дня. Каждый участок генома при этом прочитывается 30 раз для повышения точности полученных данных.
Достоверность диагностики при выборе данного вида анализа повышается, если обследовать всю семью: ребенка и родителей.
Что можно получить при полногеномном секвенировании?
Этот метод позволяет обнаружить целый ряд отклонений.
Когда нужно делать секвенирование генома?
Секвенирование генома проводится в следующих случаях.
Анализ данных
В результате полногеномного секвенирования получается огромный объем данных, который требует специальной обработки. Такая обработка включает несколько этапов.
Секвенирование экзома
Секвенирование экзома – это тест для определения генетических повреждений (мутаций) в ДНК, которые являются причиной наследственных болезней, наследственных предрасположенностей или особенностей организма.
Некоторые нуклеотиды исчезают или наоборот удваиваются или заменяются. Во многих случаях это ведет к неправильному формированию организма. Это может проявляться в виде врожденных пороков или малых аномалий развития, задержке психического развития, аутизме и других формах отклонений.
Ученые считают, что полное секвенирование экзома поможет не только обнаружить болезнь, но и предсказать ход прогрессирования заболевания и вовремя начать необходимое лечение. Выявление наследуемых мутаций также важно для оценки репродуктивных рисков.
Клиническое секвенирование экзома
Полное секвенирование экзома
Этот тест включает в себя глубокий анализ 4800 клинически значимых генов, которые связаны с известными наследственными заболеваниями. Наличие обнаруженных мутаций подтверждается классическим секвенированием по Сэнгеру. При необходимости проводится поиск аналогичных мутаций у родителей.
Цель теста – исследование экзома конкретного пациента. Метод клинического секвенирования экзома подходит для обнаружения точечных мутаций, вставок, делеций, инверсий и перестановок в экзоме. Пациент получает заключение об изменениях, связанных с его заболеванием. В то же время лечащий врач может дополнительно запросить более подробную информацию, включая данные о потенциально патогенных вариантах, локализованных в хорошо изученных областях экзома.
Результаты анализируются и проверяются целой командой специалистов медиков. Отчет об обнаруженных изменениях сопровождается подробными комментариями.
Перед проведением тестирования рекомендуется дополнительная консультация врача-генетика. В таком случае пациент может убедиться в необходимости прохождения того или иного набора тестов. Также в ходе консультации рассказывается о возможных преимуществах и рисках генетического тестирования. Дело в том, что потенциальную опасность может представлять не само тестирование (оно совершенно безвредно для пациента), а информация об обнаруженных в генетическом материале отклонениях. В частности, сведения о врожденной предрасположенности к тому или иному заболеванию обычно не сообщаются лицам, не достигшим совершеннолетия. Каждая лаборатория вырабатывает свою политику поведения в подобных случаях.
Преимущества
Ход анализа
В качестве образца для анализа сдается около 10 мл крови.
Часто задаваемые вопросы
Что включает клиническое секвенирование экзома?
Клиническое секвенирование экзома разделяется на несколько этапов.
Секвенирование: Диагностическое секвенирование экзома (DES) включает секвенирование примерно 20 000 генов. Это отличает его от секвенирования всего генома, поскольку метода нацелен на исследование 1-2% областей генома, кодирующих синтез белков, которые предположительно ответственны за появление примерно 85% от числа известных заболеваний. Целью DES является выявление изменений, которые определяют фенотип пациента.
Анализ и проверка: после завершения секвенирования все полученные данные пропускаются через биоинформационный конвейер и последовательно анализируются коллективом медиков. Для каждой обнаруженной альтерации проводится проверка, является ли она связанной с исследуемыми особенностями фенотипа. Потенциально связанные альтерации отправляются на ко-сегрегационный анализ.
Формирование отчета: каждый отдельный случай проходит несколько уровней медицинской проверки, и только после последней из них формируется отчет. Каждый отчет является специфическим для пробанда (человека, генетика которого исследуется) и включает проверку и анализ в том числе литературных данных. Подготовка отчета может длиться от нескольких дней до нескольких недель в зависимости от сложности исследования.
Доступные варианты секвенирования экзома:
Первый уровень (Клиническое секвенирования): Анализ примерно 4 800 клинически охарактеризованных генов. Полное секвенирование экзома пробанда. Проведение ко-сегрегационного анализа семьи для всех положительных или неоднозначных результатов.
Второй уровень (Полное секвенирование экзома): Анализ всех предоставленных генов с целью проведения поиска новых генов (порядка 20 000 генов по всей базе NCBI RefSeq). Полное секвенирование экзома семейного трио. Семейный ко-сегрегационный анализ для обнаруженных позитивных или неоднозначных результатов. Обязательное требование: минимум три образца от членов семьи. Тестирование на образцах эмбрионов не проводится.
Какие данные входят в отчет?
Общие результаты: положительный, предположительно положительный, отрицательный, неоднозначный.
Первичные сведения могут ограничиваться информацией, напрямую связанной с фенотипом. Это помогает выделить наиболее полезную для диагностики болезни информацию. Дополнительные сведения чаще содержат более подробные данные, относящиеся к экзому в целом, безотносительно связи с фенотипом.
Дополнительные сведения: Они варьируются в зависимости от предпочтений и возраста пациента. Данный отчет обсуждается отдельно. В дополнительные сведения попадают только установленные патогенетические или предположительно патогенетические альтерации. О клинически незначимых и доброкачественных альтерациях не сообщается. Дополнительные сведения передаются только пробанду. Прочие члены семьи не получают отчета с дополнительной информацией, однако носительство может быть предположено на основании результатов пробанда.
Когда следует заказывать таргетное секвенирование (целевая панель генов) вместо полного сквенирования экзома?
Перед тем, как начать клиническое секвенирования экзома, важно определить возможность использования таргетных панелей, которые разработаны в отношении некоторой группы заболеваний, например, аутизм, задержка психического развития и пр. К примеру, если в истории семьи обнаруживаются признаки одного или нескольких различных наследственных опухолевых заболеваний, то семья вполне может быть носителем опухолевого наследственного заболевания.
В таком случае более эффективным подходом может оказаться первоначальная проверка при помощи таргетных панелей нового поколения, таких как CancerNext, с целью добиться полного покрытия задействованных генов, поскольку такая проверка позволяет получить в том числе полностью отрицательный результат и исключить наличие мутаций в основных опухолевых генах.
Можно ли комбинировать секвенирование экзома с проведением иных генетических тестов (к примеру, хромосомным микроматричным анализом) в рамках одного заказа?
Мы рекомендуем вначале делать хромосомный микроматричный анализ, а затем выполнять секвенирование экзома.
Что необходимо предоставить для клинического секвенирование экзома?
Для выполнения секвенирования экзома необходимы:
Принимаются ли для тестирования материалы только пробанда, когда образцы родителей или иных родственников первой степени предоставить невозможно (к примеру, для приемных детей)?
Если для тестирования предоставляются только образцы пробанда либо предоставляется менее трех образцов от родственников первой степени, то можно заказать лишь проведение тестирования первого уровня (FTE).
Есть ли у клинического секвенирования экзома технические ограничения?
Да, ограничения существуют.
Можно ли сделать повторный анализ данных, полученных при секвенировании?
Да, мы предоставляем такую возможность.
Повторный анализ данных без взимания дополнительной платы возможен в течение двух лет после получения образцов.
Можно ли провести полное секвенирование экзома для эмбриональных образцов?
Эмбриональные образцы принимаются только в случае гибели плода. Для эмбриональных образцов доступно тестирование первого уровня (FTE).
Если вариант ДНК был пересмотрен и классифицирован иначе, получит ли врач уведомление об этом, чтобы сообщить обновленную информацию своему пациенту?
Секвенирование экзома в нашей лаборатории предполагает повторную классификацию вариантов. Получение дополнительной информации основанной на больших популяционных исследованиях помогает облегчить интерпретацию и уточнить диагноз. Наша лаборатория, как и все научное сообщество вовлечены в активную работу с целью лучшего понимания человеческого генома. Интерпретации и методы постоянно совершенствуются.
Проверяются ли новые гены?
Новые гены анализируются при условии выбора DES тестирования (клиническая диагностика экзома). Под новыми генами подразумеваются альтерации в генах, которые ранее не связывались с болезнями. В связи со сложностью анализа новых генов, клиническая диагностика экзома (DES) требует больше времени для выполнения заказа по сравнению с тестированием первого уровня экзома (FTE).
Если альтерации в новых генах уже обнаружены и описаны, все усилия направляются на изучение гена, включая координационные исследования и функциональные исследования с группами исследователей, изучающих ген, при наличии таковой возможности.
Предоставляет ли лаборатория полный список вариантов по пациенту?
Да, список предоставляется.
Примечание: не все альтерации из списка вариантов проходят подтверждение другими методами, и потому эти данные должны использоваться лишь в исследовательских целях.
Включает ли проводимое тестирование секвенирование митохондриального генома?
Если было обнаружено, что пациент является носителем мутации (или мутаций), можно ли протестировать членов его семьи?
Да, для членов семьи пациента можно провести односайтовый анализ альтераций, классифицированных как причины болезни.
Родственники первой степени и прочие родственники с тем же фенотипом проверяются в рамках ко-сегрегационного анализа, если соответствующие образцы были получены вместе с образцами пробанда для тестирования.
Биоинформатический анализ экспертного уровня:
Возможен анализ данных, предоставляемых заказчиком. Для уточнения информации свяжитесь с врачом-генетиком.
Биоинформационный анализ включает: